Pengertian Titik Didih, Titik Beku, Titik Lebur, Kalor Lebur, Kalor Beku, Kalor Uap dan Kalor Laten
Januari 11, 2016
Edit
Berikut ini merupakan pembahasan lengkap tentang Jumlah kalor ketika melebur dan menguap yang meliputi pengertian titik lebur, pengertian titik didih, pengertian kalor lebur, pengertian kalor beku, pengertian kalor laten, penurunan titik beku, pengertian titik beku, kalor lebur es, dan penurunan titik beku larutan.
Peristiwa itu disebut melebur atau mencair. Suatu zat melebur pasti memerlukan kalor. Banyaknya kalor tampak pada perubahan suhu yang terus meningkat. Ketika es melebur suhunya tidak mengalami perubahan. Suhu tetap ketika melebur disebut titik lebur.
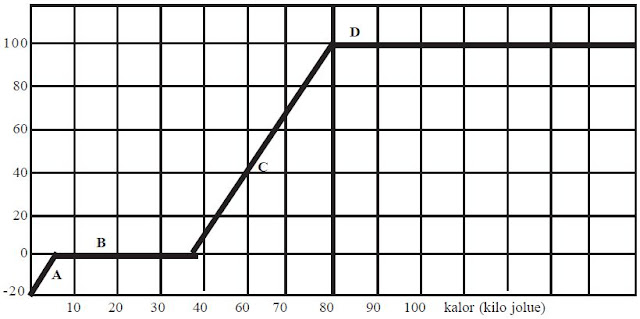
Sekalipun suhunya tetap pada saat melebur, tetapi kalornya terus meningkat. Coba kamu perhatikan grafiknya, tentukan banyaknya kalor pada saat es melebur sampai menjadi air semuanya!
Titik lebur es terjadi pada suhu 0°C. Suhu titik lebur merupakan suhu dari membekunya air menjadi es, maka titik lebur sama besarnya dengan titik beku.
Perbedaan titik lebur dengan titik beku hanya pada prosesnya. Titik lebur terjadi pada saat zat berubah dari padat ke cair, sedangkan titik beku terjadi pada saat zat berubah dari cair menjadi padat.
Banyaknya kalor yang diperlukan oleh suatu zat untuk melebur sebanding dengan massa zat dan kalor lebur zat.
Kalor lebur yaitu banyaknya kalor yang digunakan oleh setiap 1 kg zat untuk melebur pada titik leburnya. Sedangkan kalor yang digunakan untuk membeku sebanding dengan massa zat dan kalor bekunya.
Kalor beku yaitu banyaknya kalor yang dilepaskan oleh 1 kg zat untuk membeku pada titik bekunya. Kalor lebur bernilai sama dengan nilai kalor beku. Besarnya titik lebur atau titik beku dan kalor lebur atau kalor beku pada beberapa zat dapat diamati pada tabel.
Hubungan antara banyaknya kalor yang diperlukan atau dilepaskan (Q), massa zat (m), dan kalor lebur digunakan atau yang dilepaskan (L), maka akan terbentuk dalam persamaan:
Suatu zat dikatakan mendidih apabila sudah terbentuk gelembung-gelembung uap zat yang meninggalkan zat itu. Mendidihnya minyak kelapa lebih cepat dari pada air, sehingga jenis zat memengaruhi banyaknya kalor yang dibutuhkan.
Suhu didih setiap zat berbeda-beda, tergantung kepada jenis zatnya, seperti suhu air mendidih lebih tinggi dari minyak. Suhu yang dibutuhkan untuk mendidih disebut titik didih.
Apabila pemanasan terus dilakukan, suhunya tetap tidak berubah, volume air berkurang, dan terjadilah uap air dalam bentuk gas, peristiwa ini disebut penguapan.
Apabila uap air dalam gas melepaskan kalor maka akan mengembun yang membentuk air. Suhu yang dibutuhkan untuk mengembun disebut titik embun.
Besarnya titik embun sama dengan titik didih, karena dua peristiwa ini terjadi pada suhu yang sama. Dengan demikian, ketika menguap pada titik didihnya dan mengembun pada titik embunnya ternyata membutuhkan energi kalor.
Banyaknya energi kalor yang diperlukan untuk mendidih, mengembun, dan menguap bergantung kepada massa zat dan kalor uap.
Kalor uap yaitu banyaknya kalor yang dibutuhkan oleh 1 kg zat untuk menguap pada titik didihnya. Satuan kalor uap dinyatakan dengan joule per kilogram (J/kg).
Besarnya kalor uap pada beberapa zat dapat kamu amati pada tabel. Hubungan antara banyaknya energi kalor yang diperlukan untuk menguap pada titik didihnya (Q), massa zat yang akan menguap (m), dan kalor uap (U) dapat dituliskan dalam persamaan:
Pengaruh kalor tidak begitu tampak, seolah-olah tersembunyi. Oleh karena itu kalor yang tersembunyi yang digunakan untuk mengubah wujud zat seperti itu disebut kalor laten.
Baca juga: Cara Mempercepat Proses Penguapan
Jumlah Kalor Ketika Melebur dan Menguap
Berdasarkan pembahasan sebelumnya, bahwa es yang terus-menerus diberi panas akan berubah wujudnya dari padat sampai mencair semuanya.Peristiwa itu disebut melebur atau mencair. Suatu zat melebur pasti memerlukan kalor. Banyaknya kalor tampak pada perubahan suhu yang terus meningkat. Ketika es melebur suhunya tidak mengalami perubahan. Suhu tetap ketika melebur disebut titik lebur.
Sekalipun suhunya tetap pada saat melebur, tetapi kalornya terus meningkat. Coba kamu perhatikan grafiknya, tentukan banyaknya kalor pada saat es melebur sampai menjadi air semuanya!
Titik lebur es terjadi pada suhu 0°C. Suhu titik lebur merupakan suhu dari membekunya air menjadi es, maka titik lebur sama besarnya dengan titik beku.
Perbedaan titik lebur dengan titik beku hanya pada prosesnya. Titik lebur terjadi pada saat zat berubah dari padat ke cair, sedangkan titik beku terjadi pada saat zat berubah dari cair menjadi padat.
Banyaknya kalor yang diperlukan oleh suatu zat untuk melebur sebanding dengan massa zat dan kalor lebur zat.
Kalor lebur yaitu banyaknya kalor yang digunakan oleh setiap 1 kg zat untuk melebur pada titik leburnya. Sedangkan kalor yang digunakan untuk membeku sebanding dengan massa zat dan kalor bekunya.
Kalor beku yaitu banyaknya kalor yang dilepaskan oleh 1 kg zat untuk membeku pada titik bekunya. Kalor lebur bernilai sama dengan nilai kalor beku. Besarnya titik lebur atau titik beku dan kalor lebur atau kalor beku pada beberapa zat dapat diamati pada tabel.
 |
| Tabel: Titik lebur atau Titik Beku dalam °C dan Kalor Lebur atau Kalor Beku dalam J/kg |
Hubungan antara banyaknya kalor yang diperlukan atau dilepaskan (Q), massa zat (m), dan kalor lebur digunakan atau yang dilepaskan (L), maka akan terbentuk dalam persamaan:
Q = m.LSewaktu kamu memanaskan air dan minyak kelapa, ternyata minyak kelapa lebih cepat bertambah suhunya, dan apabila pemanasan diteruskan, maka akan mendidih.
Suatu zat dikatakan mendidih apabila sudah terbentuk gelembung-gelembung uap zat yang meninggalkan zat itu. Mendidihnya minyak kelapa lebih cepat dari pada air, sehingga jenis zat memengaruhi banyaknya kalor yang dibutuhkan.
Suhu didih setiap zat berbeda-beda, tergantung kepada jenis zatnya, seperti suhu air mendidih lebih tinggi dari minyak. Suhu yang dibutuhkan untuk mendidih disebut titik didih.
Apabila pemanasan terus dilakukan, suhunya tetap tidak berubah, volume air berkurang, dan terjadilah uap air dalam bentuk gas, peristiwa ini disebut penguapan.
Apabila uap air dalam gas melepaskan kalor maka akan mengembun yang membentuk air. Suhu yang dibutuhkan untuk mengembun disebut titik embun.
Besarnya titik embun sama dengan titik didih, karena dua peristiwa ini terjadi pada suhu yang sama. Dengan demikian, ketika menguap pada titik didihnya dan mengembun pada titik embunnya ternyata membutuhkan energi kalor.
Banyaknya energi kalor yang diperlukan untuk mendidih, mengembun, dan menguap bergantung kepada massa zat dan kalor uap.
Kalor uap yaitu banyaknya kalor yang dibutuhkan oleh 1 kg zat untuk menguap pada titik didihnya. Satuan kalor uap dinyatakan dengan joule per kilogram (J/kg).
 |
| Tabel: Titik Didih dalam °C dan Kalor Uap dalam J/kg |
Besarnya kalor uap pada beberapa zat dapat kamu amati pada tabel. Hubungan antara banyaknya energi kalor yang diperlukan untuk menguap pada titik didihnya (Q), massa zat yang akan menguap (m), dan kalor uap (U) dapat dituliskan dalam persamaan:
Q = m . UApabila kamu perhatikan, antara proses melebur, membeku, menguap, dan mengembun, memiliki suhu yang tidak mengalami perubahan meskipun terus diberi kalor. Kalor yang diberikan oleh api tidak menaikkan suhu, tetapi digunakan untuk mengubah wujud zat.
Pengaruh kalor tidak begitu tampak, seolah-olah tersembunyi. Oleh karena itu kalor yang tersembunyi yang digunakan untuk mengubah wujud zat seperti itu disebut kalor laten.
Baca juga: Cara Mempercepat Proses Penguapan